L’intelligence artificielle vient de décrocher le Nobel de Chimie. Ce n’est pas une métaphore : le 9 octobre 2024, Demis Hassabis et John Jumper (DeepMind) ont partagé le prix Nobel de Chimie avec David Baker (Université de Washington) pour avoir résolu l’un des grands problèmes biologiques du XXe siècle — la prédiction de la structure tridimensionnelle des protéines à partir de leur séquence d’acides aminés. Un problème sur lequel les chercheurs travaillaient depuis 50 ans.
Pour comprendre pourquoi c’est une révolution pour la médecine de la longévité, il faut saisir ce que signifie « structure protéique ».
Les protéines : les machines moléculaires du vieillissement
Notre corps est fait de quelque 20 000 protéines différentes. Elles construisent nos cellules, transportent l’oxygène, combattent les infections, transmettent les signaux nerveux. Et elles jouent un rôle central dans le vieillissement : les sirtuines (régulation épigénétique), AMPK (détection de l’énergie cellulaire), mTOR (croissance et sénescence), les télomérases — ce sont toutes des protéines dont la structure détermine la fonction.
Le problème : déterminer la structure 3D d’une protéine par cristallographie aux rayons X ou cryo-microscopie électronique prend des mois, parfois des années, et coûte des centaines de milliers d’euros. Pendant 50 ans, seule une fraction des protéines humaines avait été cartographiée.
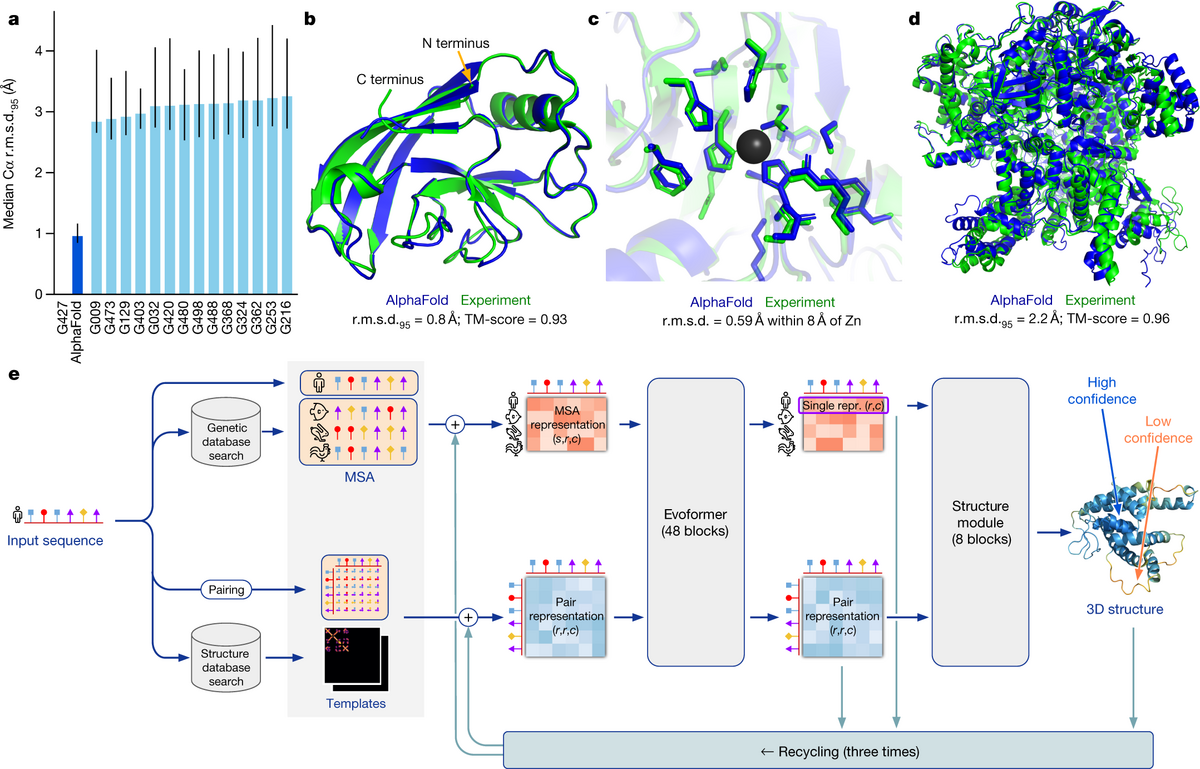
En 2020, AlphaFold 2 a prédit la structure de la quasi-totalité du protéome humain avec une précision comparable aux méthodes expérimentales. Une rupture technologique sans précédent. Mais la vraie révolution pour la découverte de médicaments est venue avec AlphaFold 3.
AlphaFold 3 : au-delà des protéines
Publié dans Nature en mai 2024, AlphaFold 3 ne prédit plus seulement la structure des protéines. Il modélise l’ensemble des molécules du vivant — protéines, ADN, ARN, ligands (petites molécules chimiques comme les médicaments), ions métalliques — et surtout leurs interactions.
C’est là que réside l’importance capitale pour la pharmacologie. Un médicament ne fonctionne que s’il se lie précisément à sa cible protéique — comme une clé dans une serrure. AlphaFold 3 prédit ces interactions avec une précision 50 % supérieure aux meilleures méthodes existantes, selon les données publiées par DeepMind.
Concrètement : là où les chercheurs testaient auparavant des milliers de molécules en laboratoire (à un coût de 10 000 à 50 000 € par molécule synthétisée), l’IA peut en cribler des millions virtuellement, en quelques heures, et ne retenir que les candidates les plus prometteuses.
Isomorphic Labs : 3 milliards de dollars sur la table
Isomorphic Labs, le spinoff de DeepMind dédié à la découverte de médicaments, ne s’est pas contenté de publier des articles. En janvier 2024, la société a annoncé des partenariats de recherche avec Eli Lilly (1,7 milliard $) et Novartis (1,2 milliard $) — soit 3 milliards de dollars de contrats signés sur des molécules qui n’existent pas encore.
Ces partenariats portent sur plusieurs maladies dont le cancer, les maladies cardiovasculaires et les maladies neurodégénératives — trois des principales causes de mortalité prématurée et d’accélération du vieillissement.
En février 2026, Isomorphic Labs a publié un rapport montrant que son propre moteur de conception de médicaments — développé au-delà d’AlphaFold 3 — multiplie par deux les performances sur les benchmarks de prédiction de liaison moléculaire. La course s’accélère.
Boltz-2 : l’open source prend le relais
Parallèlement aux acteurs privés, le MIT et la société TechBio Recursion ont publié en juin 2025 Boltz-2, un modèle open source qui prédit non seulement les structures moléculaires mais aussi l’affinité de liaison — c’est-à-dire à quel point une molécule candidate se fixe à sa cible protéique.
Les chiffres sont vertigineux : là où les méthodes de simulation physique (free energy perturbation) prenaient des semaines sur des supercalculateurs, Boltz-2 produit des résultats comparables en 20 secondes sur un seul GPU. Chez Recursion, les programmes de découverte de médicaments sont désormais bouclés en 18 mois au lieu de 42 mois.
Pour la longévité spécifiquement, cela ouvre des perspectives concrètes : identifier des molécules qui activent les sirtuines ou inhibent la sénescence cellulaire sans les effets secondaires des approches actuelles ; concevoir des sénolytiques (molécules détruisant les cellules zombies) plus précis ; modéliser l’interaction des suppléments comme la quercétine ou le resvératrol avec leurs cibles biologiques.
Ce que cela change pour nous, maintenant
Soyons honnêtes : nous ne verrons probablement pas de médicament de longévité révolutionnaire né d’AlphaFold avant 2030 au plus tôt. Le pipeline pharmaceutique prend du temps — 10 à 15 ans entre la découverte d’une molécule et son approbation, même avec l’IA.
Mais ce qui change dès maintenant, c’est la vitesse à laquelle la science de la longévité progresse. Le Prix Nobel 2024 ne récompense pas une curiosité académique : il valide une infrastructure technologique qui redessine entièrement la pharmacologie.
Des équipes comme Calico (Google), Unity Biotechnology ou Altos Labs utilisent déjà ces outils pour cibler les voies du vieillissement. Ce n’est plus de la science-fiction.
Le vieillissement est, fondamentalement, un problème de protéines qui fonctionnent mal, de structures qui se déforment, d’interactions qui dysfonctionnent. AlphaFold nous donne enfin les outils pour lire et potentiellement corriger ce code.
— Marc D.