Tu savais que t’as littéralement un deuxième cerveau dans le ventre ? Non, c’est pas du biohacking de pacotille — c’est de la science dure, publiée dans Nature, Cell et The Lancet. L’axe intestin-cerveau, ou microbiota-gut-brain axis (MGBA), c’est l’un des champs de recherche les plus explosifs de la décennie. Et en 2024, les données qui arrivent changent complètement la façon dont on pense à la dépression, à l’anxiété, et même aux troubles cognitifs.
Spoiler : tes 38 000 milliards de bactéries intestinales ne sont pas juste là pour digérer la pizza. Elles parlent directement à ton cerveau.
Le MGBA : une autoroute bidirectionnelle
L’axe intestin-cerveau, c’est pas une métaphore. C’est une infrastructure réelle de communication qui implique trois canaux principaux :
- Le nerf vague : le câble principal. Ce nerf crânien relie le tronc cérébral à l’intestin et transmet des signaux dans les deux sens. Environ 80 % des fibres du nerf vague sont afférentes — c’est-à-dire qu’elles montent de l’intestin vers le cerveau, pas l’inverse. Autrement dit, ton intestin parle plus à ton cerveau que ton cerveau lui parle.
- Le système endocrinien entérique : ton intestin produit plus de 20 hormones différentes, dont la ghréline, la leptine et le peptide YY, qui influencent l’humeur et le comportement.
- Le système immunitaire : 70 % des cellules immunitaires résident dans l’intestin. La neuro-inflammation — l’inflammation du cerveau — passe souvent par une activation immunitaire déclenchée dans les tripes.
Le chercheur John Cryan, neuroscientifique à l’University College Cork, est l’un des pionniers de ce domaine. Dans une revue de 2019 publiée dans Physiological Reviews, il documentait déjà comment les signaux microbiens modulent l’activité du cortex préfrontal et de l’amygdale — les zones du cerveau impliquées dans la régulation émotionnelle. En 2023-2024, ses équipes ont poussé encore plus loin, montrant que des souris élevées sans microbiote (germ-free) présentent des anomalies comportementales importantes, dont une réponse au stress exacerbée et une sociabilité réduite.
Les métabolites microbiens : les messagers chimiques
Le vrai game-changer, c’est la compréhension des métabolites microbiens — les molécules produites par les bactéries intestinales en fermentant ce qu’on mange.
Les acides gras à chaîne courte (AGCC)
Les AGCC — butyrate, propionate, acétate — sont produits quand les bactéries fermentent les fibres alimentaires. Le butyrate en particulier est une molécule fascinante :
- C’est la principale source d’énergie des cellules épithéliales intestinales (colonocytes)
- Il renforce la barrière intestinale, évitant le fameux leaky gut (intestin perméable)
- Il inhibe les histones désacétylases (HDACs), modulant l’expression génique dans le cerveau
- Des études récentes (2023) montrent qu’il augmente l’expression du BDNF (Brain-Derived Neurotrophic Factor) dans l’hippocampe — le facteur de croissance neuronal le plus important pour la mémoire et la résistance au stress
Une étude publiée dans Nature Communications en janvier 2024 par Valles-Colomer et al. a confirmé une corrélation forte entre des niveaux fécaux de butyrate bas et des scores de dépression élevés dans une cohorte de 1 054 participants belges.
Les précurseurs de neurotransmetteurs
C’est là que ça devient vraiment dingue. 95 % de la sérotonine corporelle est produite dans l’intestin par les cellules entérochromaffines, en réponse aux signaux microbiens. Les bactéries du genre Lactobacillus et Bifidobacterium stimulent la production de tryptophane, le précurseur de la sérotonine.
La dopamine ? Pareil. Des bactéries comme Enterococcus et Bacillus produisent de la L-DOPA, précurseur direct de la dopamine.
Et le GABA, l’acide gamma-aminobutyrique — le principal neurotransmetteur inhibiteur du cerveau, celui qui calme l’anxiété ? Certaines souches de Lactobacillus rhamnosus produisent du GABA directement. Une étude de Bravo et al. dans PNAS (2011, pionnière) montre que des souris supplémentées en L. rhamnosus JB-1 présentent moins d’anxiété et de comportements dépressifs — avec des changements mesurables dans les récepteurs GABA du cerveau.
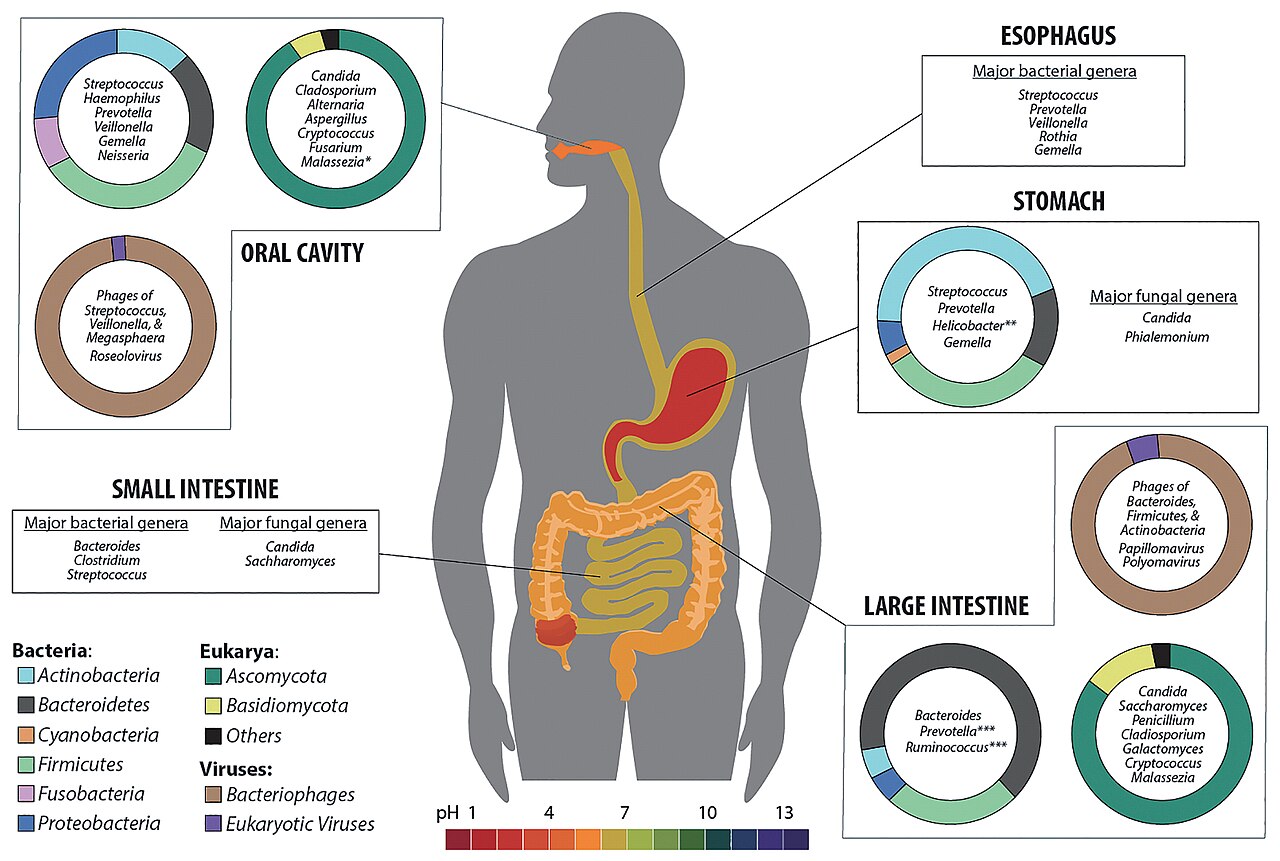
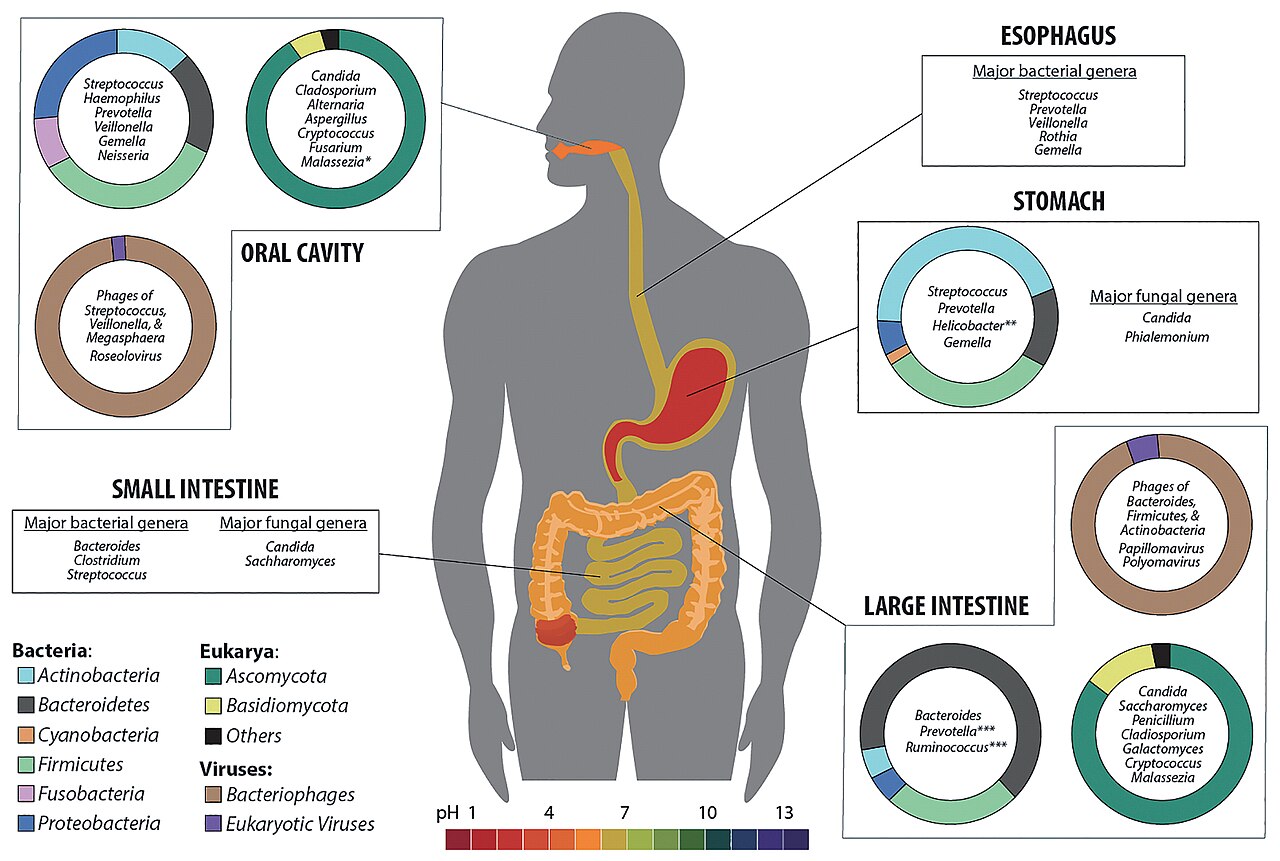
Dysbiose et dépression : les preuves s’accumulent
La dysbiose — un déséquilibre du microbiote intestinal — est maintenant associée à plusieurs troubles psychiatriques. Les études de métagénomique (séquençage de l’ADN bactérien total) permettent de cartographier ces associations avec une précision inédite.
Les données de 2023-2024
Une méta-analyse publiée dans JAMA Psychiatry en septembre 2023 a analysé 59 études portant sur 4 630 patients dépressifs versus 4 891 contrôles sains. Résultats :
- Réduction significative de Faecalibacterium prausnitzii chez les patients dépressifs (−34% en moyenne)
- Enrichissement en Eggerthella et Subdoligranulum — des bactéries pro-inflammatoires
- Diminution marquée de la diversité alpha (variété des espèces) du microbiote
Faecalibacterium prausnitzii est particulièrement intéressant : c’est l’une des bactéries les plus abondantes dans un microbiote sain, et elle produit du butyrate tout en ayant des propriétés anti-inflammatoires directes. Sa disparition est un signal d’alarme.
En 2024, une étude longitudinale du Flemish Gut Flora Project (Université de Gand) a suivi 2 100 participants pendant 5 ans. Elle a trouvé que la composition du microbiote à l’inclusion prédisait significativement le développement de symptômes dépressifs 5 ans plus tard — même après ajustement pour les facteurs de confusion habituels (alimentation, exercice, tabac).
Le cercle vicieux neuro-inflammatoire
La dysbiose déclenche une cascade inflammatoire. Les lipopolysaccharides (LPS) — des fragments de paroi bactérienne — passent dans la circulation sanguine quand la barrière intestinale est compromise. Ils activent la microglie (les cellules immunitaires du cerveau), déclenchant une neuro-inflammation qui perturbe la synthèse des neurotransmetteurs et l’hippocampogenèse (formation de nouveaux neurones dans l’hippocampe).
C’est un cercle vicieux : le stress psychologique altère le microbiote (via les glucocorticoïdes), la dysbiose augmente la perméabilité intestinale, les LPS induisent une neuro-inflammation, qui amplifie la dépression et l’anxiété.
Les approches thérapeutiques : où en est-on vraiment ?
Probiotiques et prébiotiques
Les psychobiotiques — terme inventé par Dinan, Stanton et Cryan en 2013 — désignent les probiotiques qui ont un effet mesurable sur la santé mentale. En 2024, plusieurs essais cliniques rigoureux montrent des résultats encourageants, mais nuancés.
- Une revue Cochrane de 2023 (34 essais randomisés contrôlés, 3 105 participants) conclut que les probiotiques multi-souches réduisent modérément les symptômes dépressifs (taille d’effet : Cohen’s d = 0.43) mais l’hétérogénéité des études reste un problème.
- Lactobacillus helveticus R0052 + Bifidobacterium longum R0175 : le combo le plus étudié, avec des réductions significatives d’anxiété dans plusieurs essais.
- Les prébiotiques (fructo-oligosaccharides, galacto-oligosaccharides) qui nourrissent les bonnes bactéries montrent aussi des effets sur le cortisol matinal et la vigilance aux stimuli positifs.
Mon verdict perso : les probiotiques en vente libre, c’est souvent du marketing. Les souches qui ont des données cliniques solides sont très spécifiques. Si t’es intéressé, cherche les références des souches, pas juste les milliards d’UFC.
La transplantation de microbiote fécal (TMF)
Ça sonne bizarre, et c’est bizarre. Mais la TMF — transférer le microbiote d’un donneur sain à un receveur — est devenue le traitement de référence pour les infections récurrentes à Clostridioides difficile (taux de succès > 90%).
En psychiatrie, les essais sont encore préliminaires mais fascinants. Un essai clinique à l’Université de Bâle (NCT04885374) étudie la TMF chez des patients avec dépression résistante. Les premières données de 2023 montrent une amélioration des scores HAM-D (échelle de dépression de Hamilton) chez certains patients. Pas encore de conclusions définitives, mais la direction est prometteuse.
Les synbiotiques
La combinaison probiotiques + prébiotiques — les synbiotiques — fait l’objet d’une attention croissante. L’idée : fournir à la fois les bactéries bénéfiques et leur carburant préféré. Des formulations spécifiques comme Akkermansia muciniphila + inuline sont en développement clinique pour des indications métaboliques et potentiellement psychiatriques.
L’avenir : psychobiotiques CRISPR et psychiatrie computationnelle
C’est là que ça devient science-fiction réaliste. Deux pistes me font vibrer particulièrement :
Psychobiotiques modifiés par CRISPR
Plusieurs groupes de recherche travaillent sur la modification génétique de souches bactériennes pour les transformer en véritables usines à molécules thérapeutiques. Imagine une bactérie modifiée pour produire du BDNF directement dans l’intestin, en quantité contrôlable. Le laboratoire de Timothy Lu au MIT a publié en 2023 des travaux sur des bactéries E. coli Nissle 1917 modifiées pour détecter des biomarqueurs et libérer des molécules en réponse. Le concept de “bug-as-drug” (bactérie comme médicament) progresse vite.
Psychiatrie computationnelle et microbiome
L’IA permet maintenant d’analyser les données métagénomiques à une échelle impossible il y a cinq ans. Des modèles de machine learning entraînés sur des données combinant microbiome, génomique et phénotype psychiatrique commencent à prédire les réponses aux traitements. L’équipe de Eran Segal au Weizmann Institute (Israël) a montré en 2022 que des algorithmes pouvaient prédire la glycémie post-prandiale à partir du microbiome avec une précision supérieure aux recommandations diététiques standard. Le même type d’approche s’applique maintenant aux interventions psychobiotiques.
On s’oriente vers une psychiatrie de précision où ton profil de microbiote guidera le choix du traitement.
Ce que tu peux faire maintenant
Sans attendre les psychobiotiques CRISPR, plusieurs interventions ont des données solides pour optimiser l’axe intestin-cerveau :
- Augmenter la diversité alimentaire : 30 plantes différentes par semaine (légumes, fruits, légumineuses, céréales complètes, noix) — c’est le chiffre avancé par Tim Spector (King’s College London) basé sur les données du British Gut Project.
- Fibres fermentescibles : chicorée, artichaut, ail, poireau, banane verte — les prébiotiques naturels qui nourrissent F. prausnitzii et ses copains.
- Aliments fermentés : kéfir, kimchi, choucroute non pasteurisée, miso. Une étude de Stanford (2021, Cell) a montré qu’une alimentation riche en fermentés pendant 10 semaines augmentait la diversité microbienne et réduisait 19 marqueurs inflammatoires.
- Limiter les ultra-transformés : les émulsifiants comme la lécithine de soja industrielle et la carboxyméthylcellulose altèrent la couche de mucus intestinale et favorisent la dysbiose.
- Exercice régulier : l’exercice augmente directement la diversité microbienne et la production de butyrate. Ce qu’on avait exploré dans notre article sur l’exercice et la longévité est directement pertinent ici — le mouvement n’est pas que pour les muscles.
Conclusion
L’axe intestin-cerveau n’est plus une curiosité académique. C’est un changement de paradigme. On pensait que la dépression était d’abord un problème de neurotransmetteurs cérébraux ; on réalise qu’elle est aussi — et peut-être surtout — un problème de microbiote, d’inflammation et de communication intestin-cerveau.
Ça remet en question des décennies d’approche purement pharmacologique de la psychiatrie. Et ça ouvre des pistes thérapeutiques passionnantes, des psychobiotiques ciblés jusqu’à la médecine personnalisée guidée par le séquençage.
Moi, depuis que j’ai plongé dans ce sujet, j’ai changé mon approche du fermenté et des fibres. Le kéfir le matin, c’est pas une lubie wellness — c’est de l’evidence-based nutrition. Et franchement, ça change quelque chose.
La prochaine fois que tu te sens anxieux ou dans le creux, pense à tes bactéries. Elles t’envoient peut-être un message.
— Theo R.