En 2016, le biologiste japonais Yoshinori Ohsumi a recu le prix Nobel de physiologie ou medecine pour ses decouvertes sur les mecanismes de l’autophagie. Ce mot — du grec auto (soi-meme) et phagein (manger) — designe le processus par lequel une cellule devore et recycle ses propres composants endommages. C’est le systeme de maintenance le plus fondamental du vivant.
La comprehension de l’autophagie a transforme notre vision du vieillissement, du cancer et des maladies neurodegeneratives. Et elle a suscite un interet massif pour le jeune intermittent. Mais comme souvent, la realite est plus nuancee que les titres.
Les travaux d’Ohsumi : de la levure a nous
Dans les annees 1990, Ohsumi a utilise la levure de boulanger (Saccharomyces cerevisiae) pour identifier les genes essentiels a l’autophagie — les genes ATG (autophagy-related genes). En affamant des levures mutantes et en observant leurs vacuoles au microscope, il a identifie 15 genes sans lesquels l’autophagie ne pouvait pas se produire.
La decouverte fondamentale : une machinerie moleculaire similaire existe dans toutes les cellules eucaryotes, y compris les notres. Les genes ATG de la levure ont des equivalents directs chez l’humain. L’autophagie est un mecanisme conserve depuis plus d’un milliard d’annees d’evolution.
Comment fonctionne l’autophagie
Le processus se deroule en plusieurs etapes :
-
Initiation : un signal de stress (manque de nutriments, dommages cellulaires, infection) active le complexe ULK1, qui declenche la cascade autophagique.
-
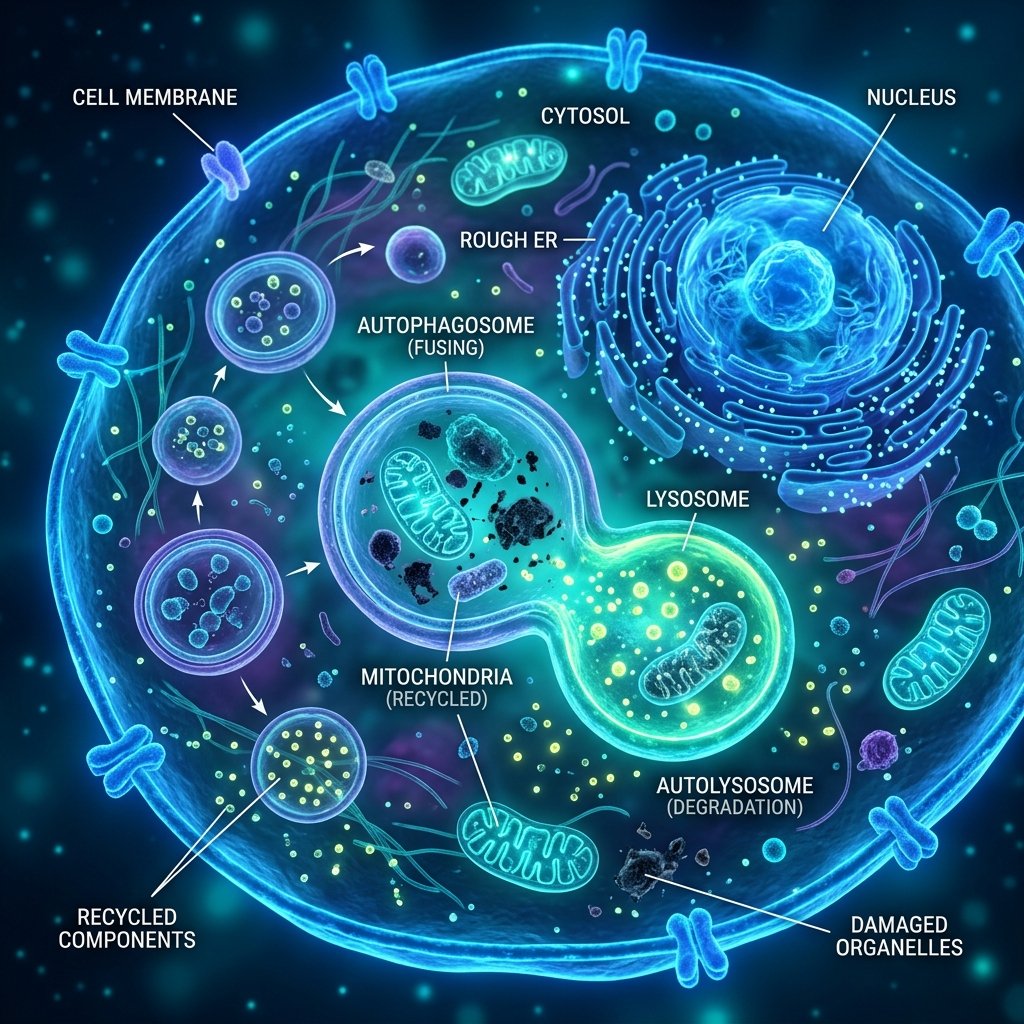
Formation du phagophore : une double membrane commence a se former autour du materiel a degrader — proteines mal repliees, mitochondries dysfonctionnelles, agents pathogenes intracellulaires.
-
Maturation de l’autophagosome : la membrane se referme completement, enfermant le contenu dans une vesicule a double membrane appelee autophagosome.
-
Fusion avec le lysosome : l’autophagosome fusionne avec un lysosome (un organite rempli d’enzymes digestives), formant un autolysosome.
-
Degradation et recyclage : les enzymes lysosomales degradent le contenu. Les acides amines, les acides gras et les nucleotides liberes sont recycles pour construire de nouvelles proteines et membranes.
C’est un systeme de controle qualite remarquablement elegant : la cellule identifie ses composants defectueux, les isole, les detruit et reutilise les materiaux.
La voie mTOR/AMPK : le thermostat central
L’autophagie est regulee par deux voies de signalisation antagonistes :
mTOR (mechanistic Target of Rapamycin) est le maitre du mode « croissance ». Quand les nutriments abondent — glucose, acides amines, insuline — mTOR est actif et l’autophagie est inhibee. La cellule est en mode construction, pas en mode nettoyage.
AMPK (AMP-activated Protein Kinase) est le detecteur de deficit energetique. Quand les reserves energetiques baissent, AMPK s’active, inhibe mTORC1 et active directement le complexe ULK1, declenchant l’autophagie.
Le jeune inverse la balance : moins de nutriments → moins d’insuline → mTOR inactive → AMPK activee → autophagie declenchee.
Le jeune comme declencheur : que disent les preuves ?
C’est ici qu’il faut etre rigoureux, car l’enthousiasme populaire pour le jeune depasse souvent les donnees.
Chez l’animal, les preuves sont solides. La restriction calorique et le jeune intermittent augmentent l’autophagie dans de nombreux tissus et sont associes a une augmentation de la duree de vie chez les levures, les vers, les mouches et les souris.
Chez l’humain, les donnees sont plus limitees :
-
Une etude sur des volontaires sains a montre qu’apres 36 heures de jeune, l’autophagie musculaire etait « modestement affectee ». Ce n’est pas rien, mais ce n’est pas l’explosion suggeree par certains influenceurs.
-
Apres 72 heures de jeune, la phosphorylation de mTOR etait reduite d’environ 50 %, et le marqueur autophagique LC3B-II augmentait d’environ 30 %.
-
Un essai clinique randomise sur un regime mimetique de jeune (FMD, Fasting-Mimicking Diet, 5 jours ProLon) a montre une augmentation mesurable du flux autophagique, avec perte de poids, baisse de la glycemie a jeun et amelioration de la sensibilite a l’insuline.
La conclusion honnete : le jeune active bien l’autophagie chez l’humain, mais les effets sont plus modestes et plus lents que ce que suggerent les etudes animales. Un jeune de 16 heures (type 16:8) produit probablement un effet autophagique reel mais modere. Un jeune prolonge (24-72h) ou un FMD produit des effets plus marques, mais avec des contraintes pratiques evidentes.
L’exercice aussi active l’autophagie
Le jeune n’est pas le seul declencheur. L’exercice physique est un puissant activateur de l’autophagie dans le muscle squelettique et d’autres tissus.
Les marqueurs autophagiques augmentent immediatement apres des periodes courtes d’exercice intense, mais aussi au cours de sessions prolongees d’intensite moderee — ce qui rejoint l’interet de l’entrainement en Zone 2 pour la longevite.
L’exercice active l’AMPK (via la depletion d’ATP) et inhibe mTOR, le meme mecanisme que le jeune. En fait, combiner exercice a jeun pourrait avoir un effet synergique sur l’autophagie, bien que les preuves directes chez l’humain restent limitees.
Autophagie et maladies
Un deficit d’autophagie est implique dans de nombreuses pathologies :
- Maladies neurodegeneratives : Alzheimer, Parkinson, Huntington — l’accumulation de proteines mal repliees (beta-amyloide, alpha-synucleine) est en partie due a un defaut de nettoyage autophagique.
- Cancer : l’autophagie joue un double role — elle previent la transformation cancereuse (en eliminant les composants endommages) mais peut aussi aider les tumeurs etablies a survivre au stress metabolique.
- Infections : l’autophagie est un mecanisme de defense contre les bacteries et virus intracellulaires (on parle de « xenophagie »).
- Vieillissement : le declin de l’autophagie avec l’age est correle a l’accumulation de dommages cellulaires et a la senescence.
Ce que ca implique concretement
L’autophagie n’est pas un interrupteur on/off — c’est un processus continu, modulable. Voici ce que les preuves actuelles soutiennent :
- Le jeune intermittent (16:8 ou 18:6) est une approche raisonnable pour stimuler moderement l’autophagie au quotidien
- Les jeunes prolonges (24-72h) ou les FMD produisent des effets plus marques mais doivent etre supervises medicalement
- L’exercice regulier (surtout endurance) est un activateur d’autophagie bien documente
- La restriction calorique meme legere (10-15 % de deficit) active partiellement les voies autophagiques
- Certaines molecules comme la rapamycine et le spermidine activent l’autophagie dans des modeles precliniques, mais les essais humains sont encore precoces
L’autophagie est un rappel que nos cellules possedent des systemes de reparation extraordinairement sophistiques. Ohsumi a mis en lumiere la machinerie. A nous de lui donner les conditions pour fonctionner.
— Marc D.